Para quienes trabajan en el sector de la fabricación, nos esforzamos por alcanzar esos márgenes y hacer todo lo posible por ser lo más eficientes posible. Pero, por supuesto, no tenemos la intención de producir productos de baja calidad, sino simplemente productos con la mejor relación calidad-precio. Aunque las intenciones siempre son admirables, sigue siendo un requisito regulatorio seguir las mejores prácticas y los SOP / instrucciones de trabajo de organismos oficiales gubernamentales como la FDA.
Una de estas normativas que hace referencia especialmente a los sectores de fabricación de alimentos, ciencias de la vida y dispositivos médicos es Current Good Manufacturing Practices (cGMP). De nuevo, se trata de una norma que ayuda a garantizar que los productos fabricados sean seguros para el consumo. Como seguimos oyendo, incluso recientemente en las noticias, que los contaminantes siguen encontrando la forma de llegar a nuestros productos alimentarios, es más prudente que nunca adherirse a este tipo de normas para, como mínimo, garantizar la seguridad y, como máximo, asegurar una reputación fiable y de confianza.
A continuación, analizaremos en mayor profundidad cGMP y cómo la tecnología puede ayudar a cumplir sus requisitos.
¿De qué trata cGMP?
cGMP abarca todo tipo de fabricación, aunque a menudo se pone el foco en la fabricación farmacéutica y alimentaria debido a que sus productos son consumidos por personas. Es un conjunto de mejores prácticas y normativas que la FDA ha considerado necesarias para cubrir todo, desde la supervisión y el control de la fabricación hasta el diseño adecuado del proceso y de las instalaciones.
Un ejemplo típico en la producción farmacéutica es que deben existir métricas claras que muestren la potencia y la pureza del medicamento, así como qué tipo de medicamento es. La calidad general también debe poder identificarse fácilmente con el sistema adecuado. Todo esto comienza desde la base, comprobando la calidad y la pureza de todos los compuestos e ingredientes en bruto necesarios para fabricar el medicamento.
Este nivel de control implica contar con un SOP claro en cada etapa de la fabricación como sistema de verificación. También debe contar con un excelente sistema de registro para cada capa utilizada y poder generar fácilmente registros electrónicos de lote cuando sea necesario. La recopilación de datos también debe combinarse con pruebas constantes de todos los equipos y la maquinaria para detectar cualquier problema de producción.
Estas comprobaciones y controles constantes detectan cualquier desviación en la producción, además de vigilar si algún contaminante ha entrado accidentalmente en el proceso de fabricación, ya sea por maquinaria defectuosa o por productos de calidad insuficiente.
¿Cuáles son las diferencias clave entre GMP y cGMP?
A primera vista, hay muy pocas diferencias entre GMP y cGMP. Si cumple con GMP, entonces su proceso y procedimiento operativo cumplen por el momento. Es el estándar mínimo necesario y puede considerarse más rentable que seguir las normas cGMP. Sin embargo, no deje que ese sea un factor decisivo importante, ya que cumplir con cGMP es una estrategia mucho mejor a largo plazo.
El cumplimiento de cGMP consiste en preparar los estándares para el futuro y trabajar para cumplir con las normativas más recientes disponibles. Es un sistema actualizado que conlleva una inversión significativa y la implantación de soluciones con un fuerte componente tecnológico. Aunque estas mejoras tecnológicas parezcan tener un coste elevado, van más allá de simplemente garantizar el cumplimiento de cGMP y ayudarán al resultado operativo global. Esto se debe a que todo el proceso de fabricación tiende a optimizarse y mejorarse como resultado de implantar el cumplimiento y los estándares regulatorios de cGMP.
Su sistema de gestión de calidad será mucho más sólido y, por tanto, más valioso al optar por el cumplimiento de cGMP.
¿Cuáles son los requisitos del cumplimiento de cGMP?
El conjunto de estándares sigue principalmente las normas y regulaciones 21 CFR. Todas ellas tienen sus propios requisitos más específicos que, una vez cumplidos por completo, constituyen el cumplimiento de cGMP. Esta amplia gama de requisitos ayuda de forma efectiva a gestionar mejor una planta de fabricación, cubriendo los aspectos físicos de equipos bien gestionados, la formación adecuada y los sistemas correctos de gestión de registros y de calidad.
Instalaciones y equipos de fabricación– el área donde se lleva a cabo la fabricación, es decir, la instalación, debe mantenerse adecuadamente para todas las actividades que se realizan. Esto significa crear un entorno de trabajo seguro para quienes trabajan allí. Además, la propia estructura debe encontrarse en buenas condiciones, al igual que la limpieza general de toda la instalación de fabricación. Después está el equipo utilizado para fabricar los medicamentos, que debe comprobarse constantemente para garantizar una calibración correcta, condiciones higiénicas y un programa de mantenimiento adecuado.
Personas implicadas en la fabricación – el personal debe estar debidamente formado en todos los aspectos de la instalación y en el uso de su equipo específico. Debe recibir formación adicional cuando se amplían sus responsabilidades o se incorpora nuevo equipo. Además, debe seguir prácticas específicas de salud y seguridad para mantenerse higiénico y conservar los productos lo más limpios posible.
Materiales utilizados – todos los materiales utilizados en el proceso de fabricación, especialmente en la elaboración de medicamentos, deben almacenarse correctamente y cumplir con las normas de higiene. La fórmula maestra de cualquiera de los medicamentos fabricados debe almacenarse adecuadamente y ser fácilmente accesible. La fabricación debe seguir la fórmula maestra en todo momento, y esto debe verificarse. No se permite ninguna desviación en ningún caso, ya que eso podría cambiar inherentemente el producto.
Un procedimiento adecuado – Todo ello debe seguir un SOP uniforme en todos los aspectos de la fabricación. Desde el mantenimiento y la limpieza de los equipos hasta el envasado y la distribución de los medicamentos a proveedores y farmacias, todo ello debe estar bien documentado, y todas las personas deben estar plenamente formadas en los procedimientos existentes y actualizados. Todos los procesos y procedimientos deben revisarse periódicamente para garantizar que se incorporen todas las novedades o aspectos relevantes de los sectores de fabricación, ciencia o gestión de calidad.
En última instancia, los procesos y procedimientos deben poder reproducirse fácilmente a diario, sin necesidad de nada especializado para respaldar esa operación. También deben ser fiables y garantizar un resultado y una producción constantes, lo que significa que haya una desviación mínima o nula en la calidad de la producción y que el flujo del proceso no tenga que modificarse o adaptarse de forma continua.
Esto garantiza que los productos fabricados el día 1 sean los mismos que los elaborados años después, gracias a la gestión de calidad implantada y al cumplimiento del proceso integrado y bien documentado.
Mantener este tipo de cumplimiento exige permanecer vigilante. No basta con implantar un sistema. Asegúrese de que determinadas personas clave tengan la responsabilidad adecuada sobre cada proceso. Además, por motivos de seguridad, solo unas pocas personas deben tener la capacidad de modificar o actualizar registros a posteriori. Esto debe ir acompañado de prácticas generales de integridad de datos, como ALCOA o ALCOA+. Esto significa disponer de un conjunto completo de datos, con un historial trazable y auditable.
Por qué el software es un componente clave en cGMP
Para facilitar mejor todo el cumplimiento, las pruebas y la gestión de registros, trabajar con el tipo adecuado de solución tecnológica será imprescindible para lograr cGMP. Además, conviene que sus sistemas sean dinámicos y crezcan junto con los cambios constantes del entorno.
Uno de los mejores puntos de partida con la tecnología es el componente central del cumplimiento de cGMP: la transparencia y la trazabilidad del producto. Disponer del historial electrónico adecuado para ver rápidamente el origen de cada materia prima utilizada para fabricar el medicamento ayuda a crear una pista de auditoría en caso de incidente o accidente.
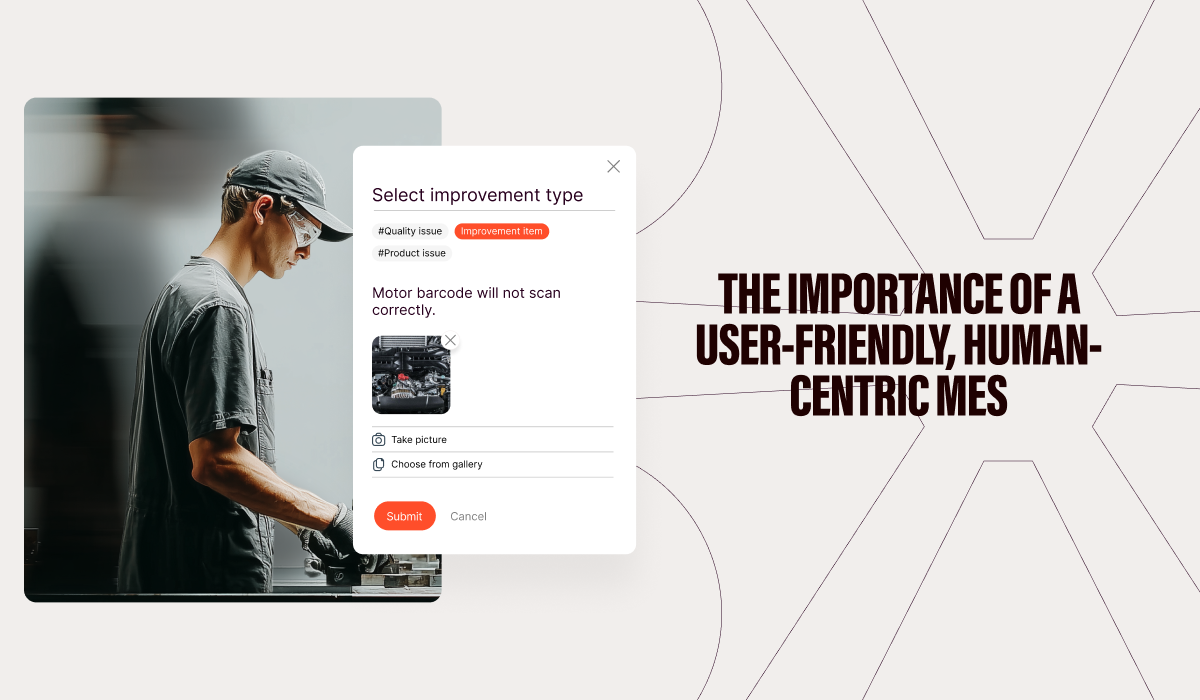
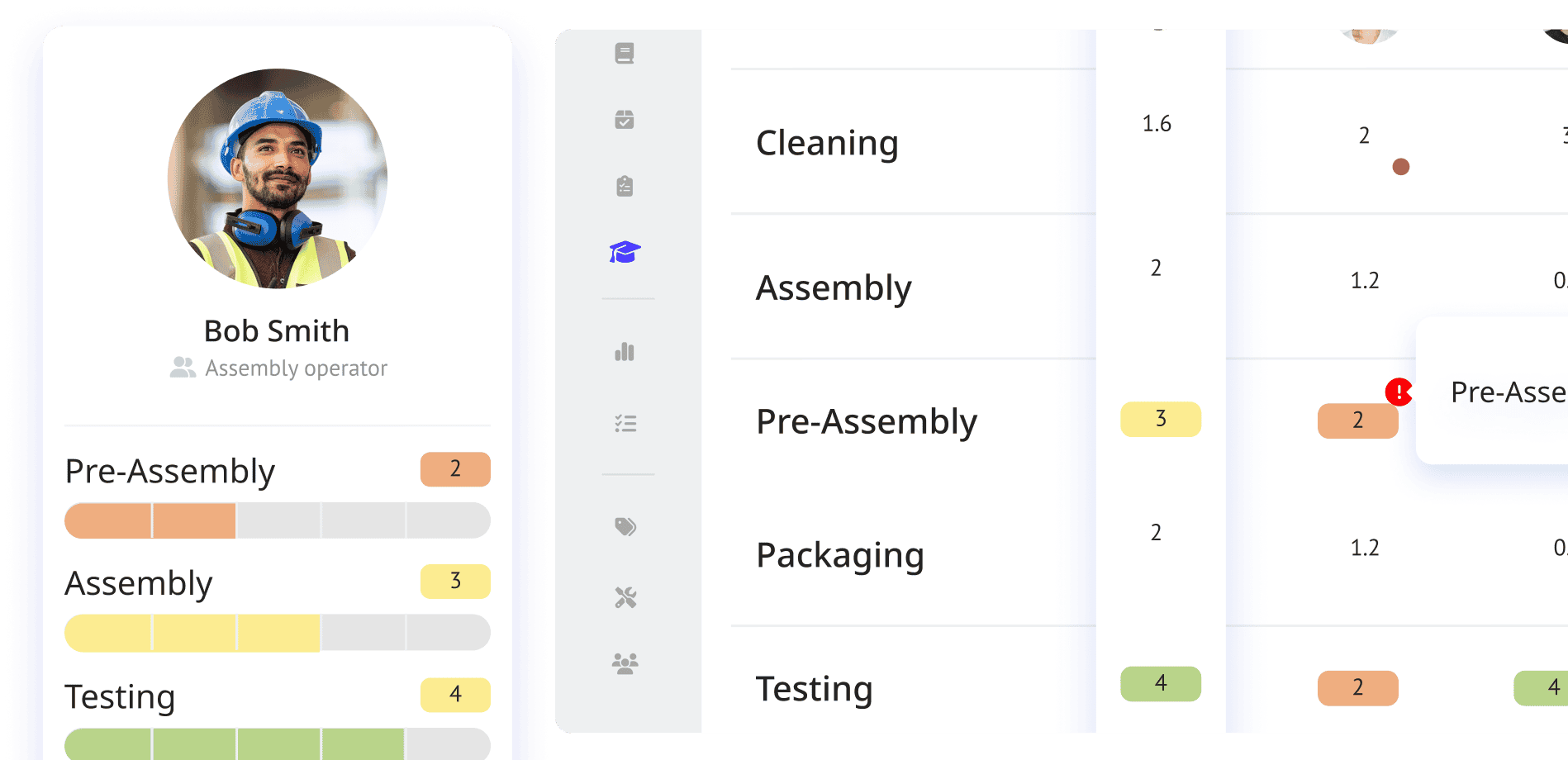
Después, todo consiste en garantizar que el SOP sea correctamente asimilado por el personal mediante sistemas de formación interactivos y en hacer seguimiento de esa formación a través de sistemas de e-learning integrados. Puede ayudar mediante aprendizaje visual y práctico, algo que a menudo se pierde en la formación más tradicional basada en papel. También existen formas de hacer seguimiento del trabajo que se realiza, ya sea durante una sesión de formación o en una jornada normal, para ver cómo se ajusta al SOP y al proceso real de ese paso específico.
Un SOP digital también ayuda a mostrar exactamente cómo hacer algo mediante la combinación de elementos visuales, vídeo y texto, lo que permite una asimilación más fácil y una ubicación digital centralizada desde la que publicar actualizaciones cuando sea necesario. Esto también ayuda cuando algo falla y quienes están en planta necesitan resolverlo de inmediato. Se asemeja a un sistema de mapeo digital que permite ver fácilmente si el problema está en la máquina o proceso actual, o si procede de otro lugar.
Este tipo de integración digital completa en el proceso general también ayuda en lo que respecta a la recopilación de datos. Eso significa cumplir también con los registros electrónicos de lote y con la gestión de registros digitales derivada de 21 CFR parte 11. Obtener cada dato no solo ayuda con el cumplimiento, sino que también ayuda a toda la organización a tomar decisiones basadas en datos.
Cómo puede ser un sistema de gestión de calidad
Ahora que sabemos lo beneficioso que puede ser poner en marcha un sistema de gestión de calidad, no solo para cumplir con las normativas cGMP sino también para las operaciones del negocio, todo consiste en encontrar el tipo de herramienta adecuado que pueda respaldar la empresa más allá del cumplimiento.
Ahí es donde entra Azumuta. Está diseñado para ayudar a alcanzar este nivel de cumplimiento y digitalizar por completo todos los aspectos de la planta de fabricación. Se ha creado con una visión holística para cubrir desde las instrucciones de trabajo digitales hasta las auditorías, la formación y las verificaciones de competencias. También se ha desarrollado para poder conectarse fácilmente a sistemas de terceros e integrarse por completo en la arquitectura del sistema.