Pour les acteurs de l’industrie manufacturière, nous nous efforçons d’atteindre ces marges et de faire de notre mieux pour être aussi efficaces que possible. Mais, bien sûr, nous n’avons pas l’intention de produire des produits de mauvaise qualité, seulement des produits offrant le meilleur rapport qualité-prix. Si les intentions sont toujours admirables, il reste néanmoins obligatoire, d’un point de vue réglementaire, de suivre les bonnes pratiques et les SOP / instructions de travail émises par des organismes officiels tels que la FDA.
L’une de ces réglementations qui concerne particulièrement les secteurs de la fabrication alimentaire, des sciences de la vie et des dispositifs médicaux est les Current Good Manufacturing Practices (cGMP). Là encore, il s’agit d’une norme qui contribue à garantir que les produits fabriqués sont sûrs à consommer. Comme nous continuons à l’entendre, y compris récemment dans l’actualité, des contaminants trouvent encore leur chemin dans nos produits alimentaires ; il est donc plus prudent que jamais de respecter ce type de normes afin, au minimum, d’assurer la sécurité et, au mieux, de garantir une réputation fiable.
Ci-dessous, nous examinerons plus en profondeur les cGMP et la manière dont la technologie peut aider à satisfaire aux exigences.
Qu’est-ce que les cGMP ?
Les cGMP couvrent tous les types de fabrication, même si l’accent est souvent mis sur les industries pharmaceutique et agroalimentaire, car les produits sont consommés par des personnes. Il s’agit d’un ensemble de bonnes pratiques et de réglementations que la FDA considère comme nécessaires pour couvrir tous les aspects, depuis la surveillance et le contrôle de la fabrication jusqu’à la conception appropriée du procédé et des installations.
Un exemple typique dans la production pharmaceutique est la nécessité de disposer d’indicateurs clairs montrant la puissance et la pureté du médicament, ainsi que le type de médicament concerné. La qualité globale doit également être facilement identifiable avec le bon système. Tout cela commence à la base, en vérifiant la qualité et la pureté de tous les composés bruts et ingrédients nécessaires à la fabrication du médicament.
Ce niveau d’exigence implique de disposer d’une SOP claire à chaque étape de la fabrication, comme système de contrôle. Il doit également y avoir un excellent système d’enregistrement pour chaque couche utilisée, capable de produire facilement des dossiers de lot (électroniques) lorsque cela est nécessaire. La collecte de données doit aussi être associée à des tests réguliers de tous les équipements et machines afin de détecter tout problème de production.
Ces contrôles et contrepoids réguliers permettent d’identifier tout écart dans la production et de surveiller si des contaminants sont accidentellement entrés dans le processus de fabrication, que ce soit via une machine défectueuse ou des produits de qualité insuffisante.
Quelles sont les principales différences entre GMP et cGMP ?
À première vue, il existe très peu de différences entre GMP et cGMP. Si vous êtes conforme aux GMP, alors votre processus et vos procédures opérationnelles sont conformes pour le moment. Il s’agit du standard minimum nécessaire et cela peut être perçu comme plus rentable que le respect des normes cGMP. Cependant, ne laissez pas cet argument être déterminant, car la conformité cGMP constitue une bien meilleure stratégie à long terme.
La conformité cGMP consiste avant tout à pérenniser les standards et à travailler selon les réglementations les plus récentes. Il s’agit d’un système actualisé qui nécessite un investissement important et l’installation de solutions technologiques avancées. Bien que ces améliorations technologiques puissent sembler coûteuses, elles vont au-delà de la simple conformité cGMP et contribuent à améliorer la performance opérationnelle globale. En effet, l’ensemble du processus de fabrication tend à être rationalisé et amélioré grâce à la mise en place des standards de conformité et de réglementation cGMP.
Votre système de gestion de la qualité n’en sera que plus robuste et donc d’autant plus pertinent dans une démarche de conformité cGMP.
Quelles sont les exigences de la conformité cGMP ?
Cet ensemble de normes suit principalement les règles et réglementations du 21 CFR. Chacune d’elles comporte ses propres exigences détaillées qui, une fois pleinement respectées, constituent la conformité cGMP. Cette large palette d’exigences permet concrètement de mieux gérer un atelier de fabrication, en couvrant les aspects physiques tels que des équipements bien entretenus, une formation adaptée, ainsi que des systèmes appropriés de gestion des enregistrements et de la qualité.
Installations et équipements de fabrication– la zone où la fabrication est réalisée, c’est-à-dire l’installation, doit être correctement entretenue pour toutes les activités qui y sont menées. Cela signifie créer un environnement de travail sûr pour les personnes qui y travaillent. En outre, la structure elle-même doit être en bon état, tout comme la propreté de l’ensemble du site de fabrication. Viennent ensuite les équipements utilisés pour fabriquer les médicaments, qui doivent être constamment vérifiés pour garantir un étalonnage correct, un état hygiénique et un programme de maintenance adéquat.
Personnes impliquées dans la fabrication – le personnel lui-même doit être correctement formé à tous les aspects de l’installation et à l’utilisation de son équipement spécifique. Il doit recevoir une formation complémentaire lorsque les responsabilités s’élargissent ou que de nouveaux équipements sont introduits. En plus de cela, il doit respecter des pratiques spécifiques de santé et de sécurité afin de rester dans des conditions d’hygiène adéquates et de maintenir les produits aussi propres que possible.
Matériaux utilisés – tous les matériaux utilisés dans le processus de fabrication, en particulier pour la fabrication de médicaments, doivent être stockés correctement et respecter les exigences d’hygiène. La formule maître de chaque médicament fabriqué doit être correctement conservée et facilement accessible. La fabrication doit suivre la formule maître à chaque fois, et cela doit pouvoir être vérifié. Aucun écart n’est jamais autorisé, car cela pourrait modifier intrinsèquement le produit.
Une procédure appropriée – Tout cela doit suivre une SOP uniforme couvrant tous les aspects de la fabrication. De la maintenance et du nettoyage des équipements jusqu’au conditionnement et à la distribution des médicaments aux fournisseurs et aux pharmacies, tout doit être correctement documenté, et chacun doit être pleinement formé aux procédures existantes et mises à jour. Tous les processus et procédures doivent être revus régulièrement afin de s’assurer que tout élément pertinent ou nouveau dans les domaines de la fabrication, de la science ou de la gestion de la qualité est bien intégré.
Au final, les processus et procédures doivent pouvoir être reproduits facilement au quotidien, sans nécessiter d’éléments spécialisés pour soutenir l’opération. Ils doivent également être fiables et garantir un résultat et une production constants, ce qui signifie qu’il y a peu ou pas d’écarts dans la qualité de production, et que le flux de processus n’a pas besoin d’être continuellement modifié ou adapté.
Cela permet de garantir que les produits fabriqués au jour 1 sont identiques à ceux produits des années plus tard, grâce à la gestion de la qualité mise en place et au respect du processus intégré et bien documenté.
Maintenir ce type de conformité signifie rester constamment vigilant. Cela ne s’arrête pas à la simple mise en place d’un système. Assurez-vous que certaines personnes clés disposent de la responsabilité appropriée sur chaque processus concerné. De plus, pour des raisons de sécurité, seules quelques personnes doivent pouvoir modifier ou mettre à jour les enregistrements a posteriori. Cela doit s’accompagner de pratiques générales de référence en matière d’intégrité des données, telles que ALCOA or ALCOA+. Cela signifie disposer d’un ensemble complet de données, avec un historique traçable et auditable.
Pourquoi le logiciel est un élément majeur des cGMP
Pour mieux gérer la conformité, les tests et la gestion des enregistrements, travailler avec le bon type de solution technologique sera indispensable pour atteindre les cGMP. En outre, vos systèmes doivent être dynamiques et évoluer avec les changements permanents du secteur.
L’un des meilleurs points de départ technologiques recommandés est le composant central de la conformité cGMP : la transparence et la traçabilité des produits. Disposer du bon historique électronique pour visualiser rapidement la source de chaque matière première utilisée dans la fabrication du médicament permet de construire une piste d’audit en cas d’incident ou d’accident.
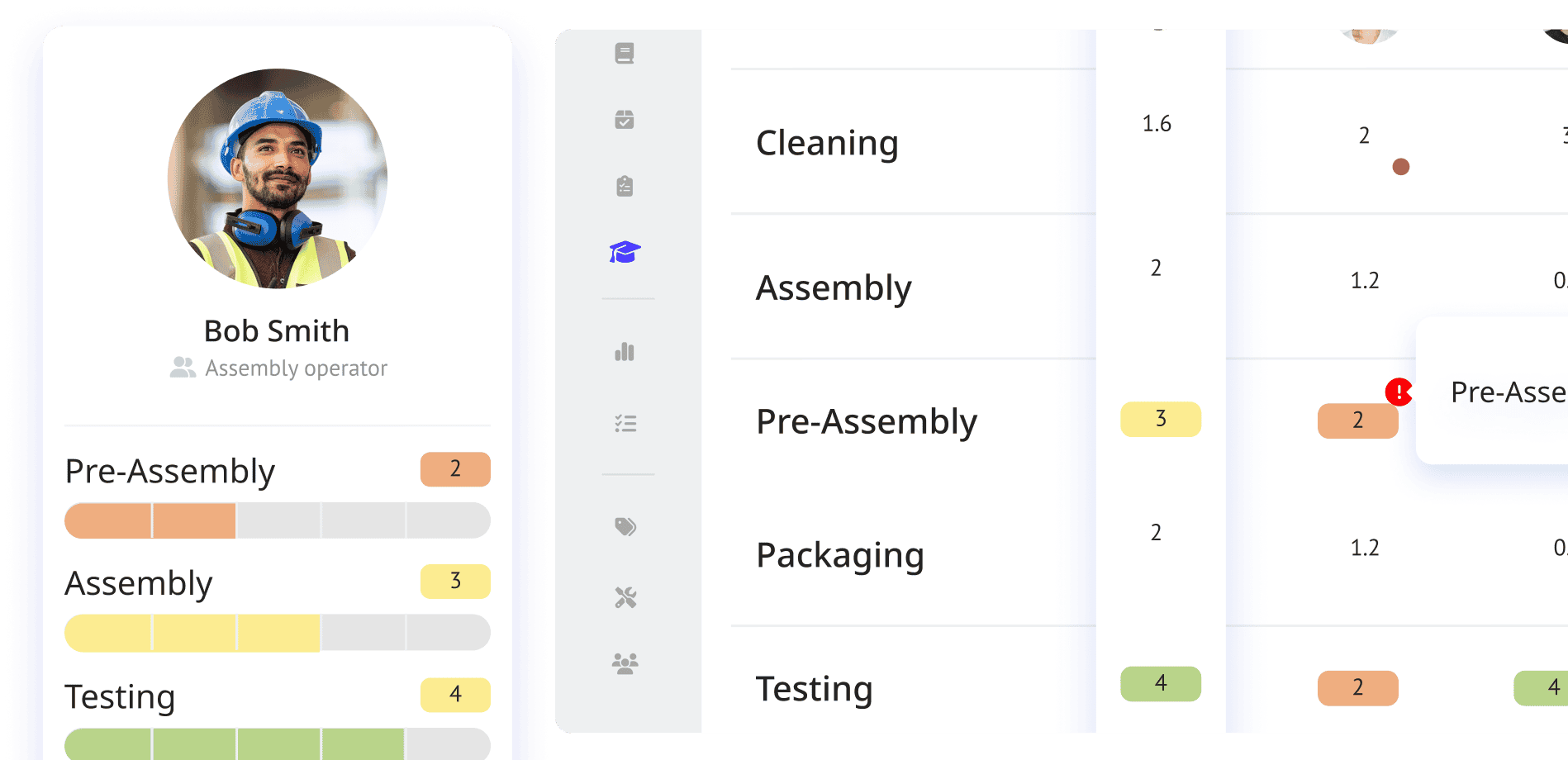
Ensuite, tout consiste à s’assurer que la SOP est correctement assimilée par le personnel grâce à des systèmes de formation interactifs, et à suivre ces formations via des systèmes d’e-learning intégrés. Cela peut aider grâce à l’apprentissage visuel et à la pratique, souvent perdus dans les formations plus traditionnelles sur papier. Il existe également des moyens de suivre le travail réalisé, que ce soit pendant une session de formation ou lors d’une journée normale, afin de voir dans quelle mesure il est conforme à la SOP et au processus réel pour cette étape spécifique.
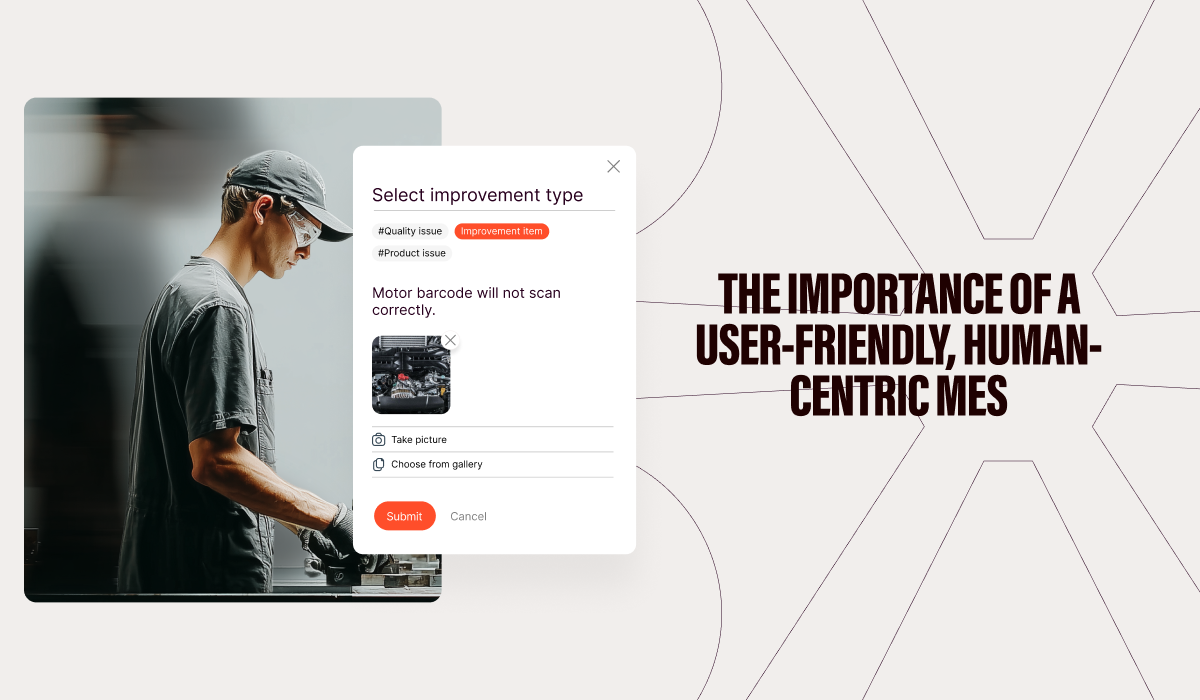
Une SOP numérique aide aussi à montrer précisément comment réaliser une tâche grâce à la combinaison de visuels, de vidéos et de texte, ce qui facilite l’assimilation et fournit un emplacement numérique centralisé pour diffuser des mises à jour lorsque nécessaire. Cela aide également lorsque quelque chose ne fonctionne pas et que les équipes sur le terrain doivent résoudre le problème immédiatement. C’est comparable à un système de cartographie numérique permettant de voir facilement si le problème se situe au niveau de la machine ou du processus actuel, ou s’il provient d’ailleurs.
Ce type d’intégration numérique complète dans l’ensemble du processus facilite aussi la collecte de données. Cela signifie être conforme aux dossiers de lot électroniques et à la gestion numérique des enregistrements issue également du 21 CFR part 11. La collecte de chaque point de donnée aide non seulement à la conformité, mais aussi l’organisation dans son ensemble à prendre des décisions fondées sur les données.
À quoi peut ressembler un système de gestion de la qualité
Maintenant que nous savons à quel point il peut être bénéfique de mettre en place un système de gestion de la qualité, non seulement pour respecter les réglementations cGMP mais aussi pour les opérations métier, tout l’enjeu consiste à trouver le bon type d’outil capable de soutenir l’entreprise au-delà de la conformité.
C’est là qu’Azumuta intervient. La solution est conçue pour aider à atteindre ce niveau de conformité et numériser entièrement chaque aspect de l’atelier de fabrication. Elle a été pensée avec une approche holistique pour couvrir tous les besoins, des instructions de travail numériques aux audits, en passant par la formation et les contrôles de compétences. Elle a également été conçue pour pouvoir se connecter facilement à des systèmes tiers afin de s’intégrer complètement à l’architecture système.